Vsebina
Z imenom atom najmanjša enota kemični elementi, ki ima svoj obstoj in je tudi nedeljiva. Atom je osnovni delček vse znane snovi in je prisoten v vseh stvareh, v živih bitjih in v inertnih predmetih.
Karakterizacija nedeljiv atom Ne zaradi nezmožnosti cepitve atoma, temveč da bi v primeru cepitve izgubil svoj atribut kemijske lastnosti: atom dejansko sestavljajo še manjši delci, znano subatomski delci.
Sestava
V bistvu sestava atoma vključuje središče, sestavljeno iz jedra, ki vsebuje protone in nevtrone, in več zunanjih lupin, ki imajo najmanjše subatomske delce atomov, elektrone.
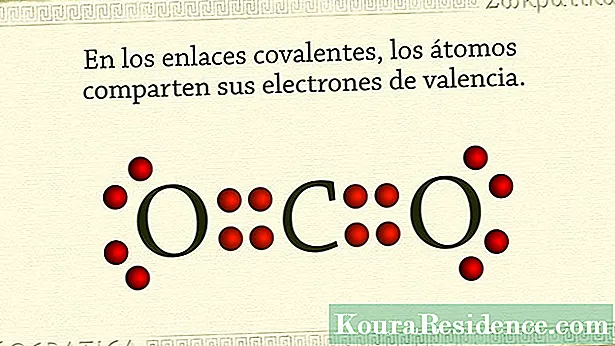
Medtem ko elektroni imajo negativni naboj, protoni enak električni naboj, vendar pozitiven in nevtroni nimajo stroškov. Bohrov model nabojev in električnih lupin dobro deluje, da razloži vezi med različnimi atomi.
Lastnosti
Atom ima vedno nekatere lastnosti, ki so koristne za razumevanje skupin, ki jih tvorijo, in različnih organizacij. Atom ima vedno a atomsko število (predstavljeno s pismom Z), ki pojasnjuje število protonov, ki jih vsebuje, kar je enako številu elektronov. Ima tudi masno število, ki ga predstavlja pismo TO, ki se nanaša na vsoto protonov in nevtronov, ki jih element vsebuje v svojem jedru.
Razvrstitev
Obstajajo različni razredi atomov in najpogostejša klasifikacija je tista, ki se izvaja v periodni sistem elementov, ki deli atome glede na njihovo atomsko število: edini element, ki ima v jedru en sam proton, je vodik.
Ti elementi so običajno tudi uvrščeni med kovine, ki imajo tendenco, da izgubijo elektrone iz zadnje lupine in nato iz. tvorijo tako imenovane pozitivne ione brez kovin Nasprotno, v zadnji plasti sprejemajo elektrone, ki tvorijo negativne ione.
Zgodovina atomske teorije
The atomska teorija razumevanje teh elementov kot minimalne enote zgradbe snovi obstaja že od antične Grčije in poleg tega Bohr Vključevalo je veliko število kemikov, ki so prispevali vprašanja v zvezi s študijo.
Leta 1803 je John Dalton atom je oblikoval tako, da je pokazal, da je bila zveza med njima narejena z določenimi določenimi predlogi. John Thomson je s svoje strani določil pozitivni in negativni naboj ter konformacijo ionov obeh znakov. Naslednji med Bohrovimi predhodniki je bil Rutherford, ki je predstavljalo vprašanje različnih ravni in elektronskih slojev.
Modeli so si sledili do trenutnih študij Kvantna teorija, usmerjena predvsem na polja. Očitno je gotovo, da je struktura atomskega jedra in delcev, ki ga sestavljajo, veliko bolj zapletena kot tradicionalna elektronska struktura atomov.
Nato popoln seznam elementov periodnega sistema, ki predstavljajo celoto sestavljenih atomov.
| Aktinij | Disprozij | Magnezij | Rodijev |
| Aluminij | Dubnium | Mangan | Roentgenio |
| Americij | Einsteinium | Meitnerius | Rubidij |
| Antimon | Erbij | Mendelevij | Rutenij |
| Argon | Scandium | Živo srebro | Rutherfordio |
| Arzen | Kositer | Molibden | Samarij |
| Astatus | Stroncij | Neodim | Seaborgio |
| Žveplo | Europium | Neon | Selen |
| Barij | Fermij | Neptunij | Silicij |
| Berilij | Flerovio | Niobij | Natrij |
| Berkelij | Fluor | Nikelj | Talij |
| Bizmut | Tekma | Dušik | Tantal |
| Bohrio | Francij | Nobelio | Tehnecij |
| Bor | Gadolinij | Zlato | Telur |
| Brom | Galij | Osmij | Terbij |
| Kadmij | Germanij | Kisik | Titan |
| Kalcij | Hafnij | Paladij | Torij |
| Kalifornij | Hassio | Srebro | Tulij |
| Ogljik | Helij | Platina | Ununoctio |
| Cerij | Vodik | Svinec | Ununpencij |
| Cezij | Železo | Plutonij | Ununseptio |
| Cink | Holmij | Polonij | Untrium |
| Cirkonij | Indijski | Kalij | Uran |
| Klor | Iridij | Praseodim | Vanadij |
| Kobalt | Kripton | Obljubi | Volfram |
| baker | Lanthanum | Protaktinij | Ksenon |
| Kopernik | Lawrencio | Radio | Jod |
| Chrome | Litij | Radon | Itterbij |
| Kurij | Livermorio | Renij | Ytrio |
| Darmstadtij | Lutecij |